


Applications des fonctions usuelles à la physique
Mouvement dans un champ de force centrale newtonien
Introduction
Soient deux points matériels A(mA,qA) et B(mB,qB).Tout se passe comme s'il n'y avait qu'un poids M(µ) soumis a un champ de force centrale (vers G), G le barycentre du système {A(mA),B(mB)}
On pose avec k =
On réalise l'étude dans le référentiel barycentrique R galliléen.
Trajectoire générale
On applique le Principe Fondamental de la Dynamique dans R à M de masse réduite µ.De cette équation il est possible d'en déduire l'équation suivante :
θ0 correspond à la direction de l'axe focal. Ce qui détermine le mouvement de M, donc A et B ont le même mouvement que M.
Si
- e=0 il s'agit d'un cercle,
 by CALLAUD Pierre
by CALLAUD Pierre - 0 < e < 1 il s'agit d'une ellipse,
 by CALLAUD Pierre
by CALLAUD Pierre - e=1 il s'agit d'une parabole,
 by CALLAUD Pierre
by CALLAUD Pierre - e>1 il s'agit d'une hyperbole.
 by CALLAUD Pierre
by CALLAUD Pierre
Deuxième principe de la thermodynamique
Enoncé
Pour tout système thermodynamique il existe une fonction appelée entropie S telle que :- S est extensible,
- S est une fonction d'état : à l'équilibre thermodynamique, S ne dépend que d'un petit nombre de paramètres d'état, indépendants du chemin suivi.
- Au cour de l'évolution d'un système fermé et calorifugé d'un état initial Ei à un état final Ef, l'entropie ne peut qu'augmenter.
Identités thermodynamiques
On a l'égalité suivante :Variation d'entropie au cours d'une transformation réversible
Pour une transformation réversible on a :Entropie de quelques fluides modèles
Phase condensée incompressible
Dans ce casdonc
Gaz parfait
Pour un gaz parfait on a :d'où
Gaz de Van Der Waals
Pour ce type de gaz on a :Distance de l’horizon en fonction de l’altitude
On peut se demander à quelle distance se trouve l’horizon en fonction de l’altitude à laquelle se trouve l’observateur (L, la longueur de l’arc de cercle en bleu sur la figue en dessous)
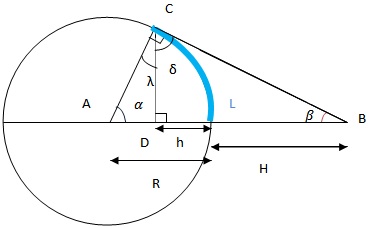
COHU Aurélien
On suppose que la terre est une sphère parfaite de rayon R
On cherche à déterminer L en fonction de la hauteur H.
Par définition d'un angle,
On cherche donc par trigonométrie à exprimer
La droite (BC) est tangente au cercle représentant la terre car C est le point le plus éloigné visible, il est par définition unique et une droite coupant un cercle en un seul point est par définition une tangente au cercle.
Donc (AC) et (BC) sont perpendiculaire. D'où le triangle ABC est rectangle en C.
Donc
Et donc
Or,
Donc
Donc

Ce(tte) oeuvre est mise à disposition selon les termes de la Licence Creative Commons Paternité - Pas d'Utilisation Commerciale 3.0 France.